美国西北大学研究发现,“渐冻症小鼠”的大脑皮层运动区产生的能量减少,且烟酰胺腺嘌呤二核苷酸(NAD+)水平降低,通过补充烟酰胺单核苷酸(NMN)维持NAD+平衡后,可改善“渐冻症小鼠”运动神经元的线粒体完整性和神经健康状态,这提示NMN或许是协助治疗渐冻症的一种新希望。
“ALS(渐冻症在医学上的简写 )如同一支点燃的蜡烛,不断融化你的神经,使你的躯体变成一堆蜡。通常它从腿部开始,然后慢慢向上发展,等你不能控制大腿肌肉的时候,你就无法再站立起来……”这是美国作家米奇·阿尔博姆在其长篇纪实小说《相约星期二》里,对渐冻症患者的疾病进展过程所进行的描述。

渐冻症,在医学上又被称为肌萎缩性侧索硬化症(amyotrophic lateral sclerosis, ALS),是一种破坏患者机体神经细胞并导致残疾甚至死亡的神经系统疾病。渐冻症通常影响患者大脑和脊髓中与运动有关的神经细胞,造成控制肌肉运动的运动神经元退化,从而让患者逐渐丧失运动、吞咽、说话甚至呼吸的能力。
大多数渐冻症患者通常在症状首次出现后的3-5年内死于呼吸衰竭。目前,渐冻症与癌症、艾滋病、白血病以及类风湿并列为“世界五大绝症”,尚无治愈方法,也缺乏有效的措施来阻止或逆转疾病的进展。
2022年3月,来自美国西北大学(Northwestern University)Hande Ozdinler副教授的研究团队分析比较了健康小鼠和呈现一种名为TDP-43病理变化的“渐冻症小鼠”的大脑皮层运动区的代谢谱,发现“渐冻症小鼠”的大脑皮层运动区产生的能量减少,且烟酰胺腺嘌呤二核苷酸(NAD+)水平降低,而通过补充烟酰胺单核苷酸(NMN)维持NAD+平衡后,可改善“渐冻症小鼠”运动神经元的线粒体完整性和神经健康状态。该研究结果提示维持NAD+平衡或许是一种治疗渐冻症的策略。目前这项研究已发表于国际权威期刊《科学报告》(Scientific Reports)上[1]。

什么原因导致肌萎缩无力?
为了厘清渐冻症疾病发生发展的原因,首先需要了解与之有关的神经系统及运动神经元的基本概念。
神经系统是人体的“中央政府”,在机体内起主导作用,可将机体内、外的各种信息进行整合并传递到机体的各个组织器官,控制和调节其生理活动,以维持机体与外界环境的相对平衡。神经系统由脑、脊髓和它们所发出的脑神经、脊髓神经组成。其中,脑和脊髓是神经系统的中枢部分,组成中枢神经系统;脑神经和脊髓神经是神经系统的周围部分,组成周围神经系统。
运动神经元是负责将脊髓和大脑发出的信息传到肌肉和内分泌腺,支配效应器官活动的神经元。神经元又叫神经细胞,是神经系统结构和功能的基本单位。神经元的基本结构包括细胞体和突起两部分。神经元的突起一般包括一条长而分支少的轴突和数条短而呈树状分支的树突。长的突起外表大都套有一层髓鞘,对轴突具有保护和绝缘的作用。
渐冻症的具体病因尚不明确,但目前已经明确的是,它是相对罕见的运动神经元病,患者的脑、脊髓中的运动神经元发生进行性退化,并伴有肌肉萎缩、 肌无力等症状,如同身体被逐渐冻住。
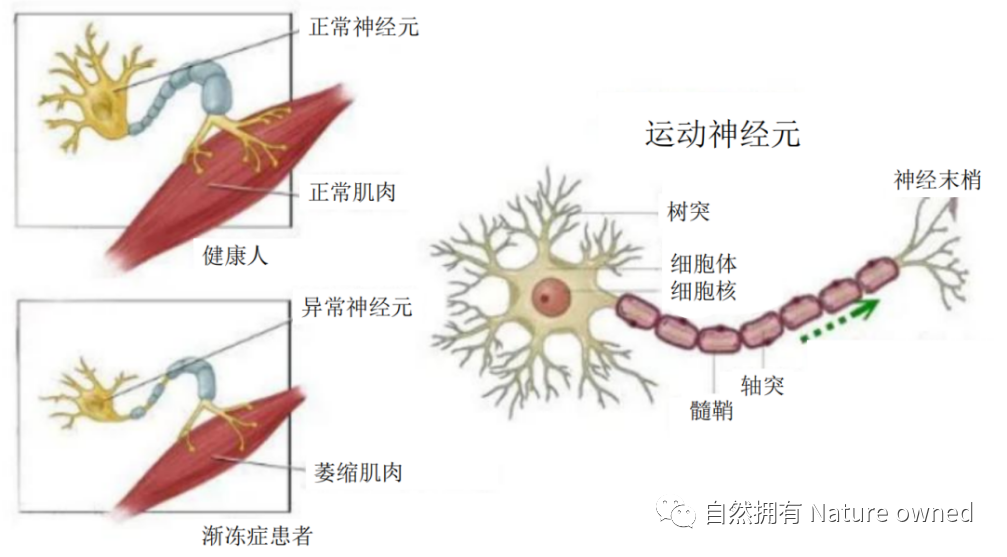
图3 渐冻症患者的运动神经元退化所致肌肉萎缩示意图
在“渐冻症小鼠”身上的发现
明确渐冻症的病因与运动神经元的损害有关后,科研人员们一直在积极寻找导致运动神经元损害的具体原因。目前的主要理论包括:(1)神经毒性物质累积在神经细胞之间,最终造成神经细胞的损伤;(2)一种名为自由基的物质使神经细胞膜受损;(3)神经生长因子缺乏,使神经细胞无法持续生长、发育。而对于“神经毒性物质累积理论”,科研人员们先后发现了许多具体的神经毒性物质,“TDP-43异常蛋白”就是其中之一[2]。
TDP-43是一种细胞核内的蛋白质,正常情况下TDP-43蛋白多分布在细胞核内发挥作用,仅少量分布在细胞质。而通过病理研究可发现,TDP-43病理变化是渐冻症患者病变区的神经元普遍发生的现象。因此,研究人员们常常将呈现TDP-43病理变化的小鼠模型视为“渐冻症小鼠”,Hande Ozdinler副教授及其同事也不例外。
研究团队注意到,渐冻症患者和“渐冻症小鼠”的疾病早期均在大脑皮层运动区出现了线粒体功能障碍(线粒体是细胞的“能量工厂”,参与能量代谢过程,主要功能是提供能量),同时渐冻症患者和“渐冻症小鼠”的病变区域均出现了TDP-43病理变化。为了明确与渐冻症TDP-43病理变化有关的代谢产物的变化规律,研究团队分析了健康和患病小鼠的运动皮层的代谢谱,发现“渐冻症小鼠”的大脑皮层运动区产生的能量减少,且烟酰胺腺嘌呤二核苷酸(NAD+)水平降低。
补充NMN可改善“渐冻症小鼠”神经健康状态

图4 NMN可改善呈现TDP-43病理变化的“渐冻症小鼠”运动神经元的健康状况
注:(a)、(b)分别表示prpTDP-43A315T-UeGFP小鼠(即“渐冻症小鼠”)未添加和添加NMN后的运动神经元代表性图像;(c)、(d)分别表示WT-UeGFP小鼠(即“健康小鼠”)未添加和添加NMN后的运动神经元代表性图像;(e)为神经元轴突的平均长度的条形图;(f)为轴突长度百分比分布;(g)为神经元突树分支程度的Sholl分析(一种定量分析神经元轴突和树突的方法)。
基于上述研究结果,研究团队提出了他们的假设:NAD+的前体物质NMN有助于维持渐冻症患者运动神经元的NAD+平衡,从而改善其神经健康。为了验证这一假设,研究团队将NMN分别添加入健康小鼠和患病小鼠的运动神经元的培养基中,通过测量神经元的轴突的平均长度和树突的分支程度来评估NMN的治疗效果。结果发现,补充NMN可改善“渐冻症”小鼠的运动神经元的健康状态。此外,研究团队借助相关光电子显微镜观察到,经过NMN处理后的运动神经元具有更完整的线粒体结构。
虽然该研究仍停留在动物实验阶段,但它强调了理解疾病早期运动皮层代谢组学问题的必要性。未来,科学家们将通过更多相关研究来验证补充MNM提高人体NAD+水平,进而改善渐冻症患者运动神经健康的可行性。
参考文献
[1] M Gautam, Gunay A, Chandel N-S, et al. Mitochondrial dysregulation occurs early in ALS motor cortex with TDP-43 pathology and suggests maintaining NAD(+) balance as a therapeutic strategy[J]. Sci Rep, 2022, 12(1): 4287.
[2] 司马旦旦,潘卫东,桂丽卿,等. 肌萎缩侧索硬化相关标志物及发病机制的研究进展[J]. 中西医结合心脑血管病杂志, 2022, 20(05): 877-879.
47


